- KAIST-서울대병원-분당서울대병원-경북대병원-국립중앙의료원-지놈오피니언 공동연구팀, 산·학·병 공동 코로나19 위험 인자 연구
- 생물정보학 및 단일세포 오믹스 기반 기저 질환이 없는 저위험군의 신규 중증 위험인자 규명
- 기저 질환이 없는 집단 내 중증 환자는 ‘클론성조혈증’ 이라는 후천적 유전자 변이가 있음을 발견
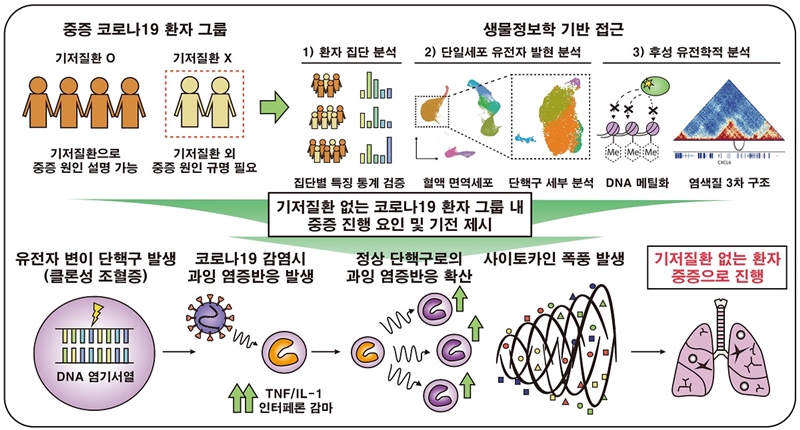
□ 그림설명: 중증 코로나19 환자 집단 중 기저 질환이 없음에도 중증으로 진행된 환자들이 존재한다. 이 환자 집단에서 중증 진행 인자를 발굴 및 검증하기 위해 생물정보학에 기반하여 세 가지 서로 다른 접근법을 사용했다. 첫 번째로, 환자의 임상 정보를 수집 후 그에 따라 집단 별로 나누어 집단 별 임상정보의 특징을 통계 기법을 통해 분석했다. 두 번째로는, 단일세포 유전자발현 분석이라는 최신의 연구기법을 적용하여 혈액 내 면역세포들의 발현 특징을 분석하였고, 특히 단핵구에 대해서 세부 분석을 진행하였다. 세 번째로는 후성 유전학측면에서의 분석으로, 분자적 기전을 제시하기 위해 단핵구의 DNA 메틸화 패턴과 염색질 3차 구조 정보를 도입 및 분석하였다. 이 세 가지 접근법을 통해 기저질환 없는 코로나19 환자 그룹 내 중증 진행 요인 및 기전을 제시했다. 중증 진행 요인으로는 유전자 염기서열에 변이가 발생한 단핵구로, 이 단핵구는 유전자 변이로 인해 염증반응을 쉽게 일으킬 수 있는 상태가 되어 코로나19 바이러스 감염 시 TNF/IL-1과 인터페론 감마(IFN-γ)를 필두로 한 과잉 염증반응을 빠르게 일으킨다. 이 과잉 염증반응이 다른 정상 단핵구들에도 퍼져나가면서 연쇄적인 염증반응을 일으켜 사이토카인 폭풍 현상이 발생하고, 결과적으로 기저질환이 없음에도 불구하고 중증으로 진행이 가능해진다.
KAIST(총장 이광형)는 생명과학과 정인경 교수 연구팀이 서울대병원 강창경, 고영일, 분당서울대병원 송경호 교수, 경북대병원 문준호 교수, 국립중앙의료원 이지연 교수, 지놈오피니언 社로 이루어진 산·학·병 공동연구를 통해 기저 질환이 없는 저위험군의 신규 코로나19 중증 위험 인자를 발굴하고, 발굴된 인자의 과잉 염증반응에 대한 분자 메커니즘을 제시했다고 29일 밝혔다.
코로나19 바이러스(SARS-CoV2)는 지난 2년이 넘도록 확산하면서 전 세계적으로 6억 명 이상이 감염됐고, 이 중 6백만 명 이상이 사망했다. 이러한 심각성으로 인해 코로나19 바이러스의 병리에 관한 연구가 활발히 진행됐고, 단핵구(큰 크기의 백혈구, Monocyte)의 과잉 염증반응으로 인한 중증 진행 메커니즘 등이 밝혀졌다.
하지만 개별 코로나19 환자마다 면역 반응의 편차가 크게 나타나는 현상에 대해서는 앞서 찾은 연구 결과만으로는 전부 설명할 수 없다. 예를 들어 중증 코로나19 환자 중에서 당뇨병이나 고혈압 등의 기저 질환이 없는 경우도 빈번하기에 이들이 코로나19 감염 시 중증으로 진행될 수 있는 신규 위험 인자를 발굴하는 것은 환자 맞춤형 치료에 있어 매우 중요하다.
KAIST 생명과학과 최백규, 박성완 석박사통합과정과 서울대병원 강창경 교수가 주도한 이번 연구에서는 기존의 기저 질환이 없는 중증 코로나19 환자의 중증 요인을 알아내기 위해, 국내 4개의 병원이 합동해 총 243명의 코로나19 환자의 임상 정보를 수집 및 분석했다. 연구팀은 그 집단의 임상적 특징을 밝히고, 단일세포 유전자 발현 분석과 후성유전학적 분석을 도입해 관찰된 임상적 특징과 중증 코로나19 내 과잉 염증반응 간의 유전자 발현 조절 메커니즘을 분석했다.
그 결과, 기저 질환이 없는 집단 내 중증 환자는 `클론성조혈증'이라는 특징을 가지고 있는 것을 관찰하였다. 이는 혈액 및 면역 세포를 형성하는 골수 줄기세포 중 후천적 유전자 변이가 있는 집단을 의미한다. 또한 단일세포 유전자 발현 분석을 통해 클론성조혈증을 가진 중증 환자의 경우 단핵구에서 특이적인 과잉 염증반응이 관찰되는 것을 확인했고, 클론성조혈증으로 인해 변화한 후성유전학적 특징이 단핵구 특이적인 과잉 염증반응을 일으키는 유전자 발현을 유도하는 것을 연구팀은 확인했다.
해외 연구단에서도 유사하게 클론성조혈증과 코로나19 간의 관련성에 주목한 연구들이 있었으나 코로나19와의 관련성을 명확히 밝히지 못했고, 과잉 염증반응으로 이어지는 분자 모델 역시 제시하지 못했다. 이에 반해 공동 연구팀은 생물정보학 기반 계층화된 환자 분류법과 환자 유래 다양한 면역 세포를 단 하나의 세포 수준에서 유전자 발현 패턴 및 조절 기전을 해석할 수 있는 단일세포 오믹스 생물학 기법을 적용해 클론성조혈증이 코로나19의 신규 중증 인자임을 명확하게 제시했다. 해당 연구 결과는 앞으로 기저질환이 없는 저위험군 환자라도 클론성조혈증을 갖는 경우 코로나19 감염 시 보다 체계적인 치료 및 관리가 필요함을 의미한다.
이번 연구 결과는 두 개의 국제 학술지, `헤마톨로지카(haematologica, IF=11.04)'에 9월 15일 字 (논문명: Clinical impact of clonal hematopoiesis on severe COVID-19 patients without canonical risk factors) 온라인 게재가 되었으며. ‘실험 및 분자 의학(Experimental & Molecular Medicine, IF=11.590)'에 지난 8월 1일 字 (논문명: Single-cell transcriptome analyses reveal distinct gene expression signatures of severe COVID-19 in the presence of clonal hematopoiesis) 게재 승인됐다.
이번 연구는 장기화된 코로나19 팬데믹 상황 속에서 연구계·의료계·산업계로 이루어진 연구팀 서로 간의 긴밀한 협력을 통해 코로나19 환자의 신규 중증 인자를 밝히고, 그에 대한 분자적 기전을 제시해 환자별 맞춤 치료전략을 제시한 연구로 중개 연구(translational research)의 좋은 예시로 평가받는다.
이번 연구를 수행한 KAIST 최백규 석박사통합과정은 "최신의 분자실험 기법인 단일세포 오믹스 실험과 생물정보학 분석 기술의 융합이 신규 코로나19 중증 환자의 아형과 관련 유전자 조절 기전을 규명 가능케 하였다ˮ며, "다른 질환에도 바이오 데이터 기반 융합 연구 기법을 적용할 것이다ˮ고 말했다.
분당서울대병원 송경호 교수는 "이번 연구는 임상 현장에서 코로나 환자별 맞춤 치료 전략을 정립하는 데 있어서 중요한 정보를 제공한 연구ˮ라며 "앞으로도 중증 코로나19 환자의 생존율을 높이기 위해 임상 정보를 바탕으로 한 맞춤 치료전략 연구를 이어나가겠다ˮ라고 밝혔다.
지놈오피니언 대표를 겸임하고 있는 서울대병원 고영일 교수는 "회사에서 개발한 클론성조혈증 탐지 및 분석 기술이 코로나19 팬데믹 해결에 도움이 되어 보람차다ˮ면서 "앞으로도 새로운 바이오마커를 발굴 및 분석하는 기술을 개발해 인류의 건강한 삶에 지속적으로 기여하고 싶다ˮ고 말했다.
한편 이번 연구는 서경배과학재단과 과학기술정보통신부의 지원을 받아 수행됐다.
□ 용어설명
1. 클론성조혈증
클론성조혈증(CHIP, Clonal hematopoiesis of indeterminate potential)은 혈액 및 면역 세포를 형성하는 골수 줄기 세포 중 후천적 유전자 변이가 있는 집단을 의미한다. 이 집단은 유전적 변이로 인해 정상 줄기세포에 비해 단핵구/대식세포(macrophage)로의 분화가 활발하게 일어나 전체 면역 세포 중 일정 비율 이상을 차지하게 된다. 변이를 가지고 분화한 면역세포의 경우 면역 반응을 관리하는 물질 분비 및 반응에 이상이 생겨 기존보다 더 강한 면역반응을 일으킨다. 현재 클론성조혈증은 심혈관계 질환 및 자가면역 질환의 새로운 원인으로서 연구 중에 있다.
2. 단일세포 유전자발현 분석
단일세포 유전자발현 분석이란 1개의 세포를 분리하여 극미량의 RNA를 증폭하고 차세대염기서열 분석법으로 시퀀싱하여 해당 세포의 유전자 발현량을 분석하는 기술이다. 이를 통해 다양한 세포를 포함한 환자 조직이나 혈액의 유전자 발현량을 동시에 분석하는 기존 분석 방식과 달리 기원이 되는 다양한 세포의 각 유전자 발현량을 정량화 할 수 있다. 본 연구에서는 세포 1개 단위로 수천개의 세포를 동시에 시퀀싱하여 개별 세포들의 유전자발현을 분석하여 환자 혈액 내 면역세포의 다양한 면역반응을 매우 깊게 연구하는데 적용되었다.
3. 후성유전학
후성 유전학은 유전자 서열에 변형 없이 염색체에 생긴 변화만으로 인한 유전자 발현 조절 기전을 연구하는 분야이다. 생물 내 세포들 간의 염기서열 정보는 사실상 동일한데, 각각의 세포들의 역할은 서로 다르다. 이는 세포 종류에 따른 선별적으로 유전자 발현이 조절되기 때문인데, 이를 연구하기 위해 생겨난 분야로, 현재는 전반적인 유전자 발현을 촉진하거나 억제시키는 분자 기전에 대해 초점을 맞춘다. 예시로 DNA 염기서열 정보는 변화시키지 않고 사이토신(Cytosine)에 메틸기(Methyl group)만 붙이는 DNA 메틸화, 핵 내의 공간상의 거리를 통해서 유전자 발현을 조절하는 염색질 3차구조 등이 예시이다.
4. 과잉 염증반응
사이토카인 폭풍이라고도 불리며, 본래 병원균으로부터 인체를 방어하는데 필요한 염증반응이 너무 과도하여 오히려 인체 조직에 해를 입히는 현상을 의미한다. 과도한 염증반응은 류마티스 관절염이나 루푸스와 같은 자가면역질환에서도 관찰되며, 정상적인 조절을 벗어난 사이토카인 및 그에 대한 반응의 증가가 공통적인 특징이다.
5. 실험 및 분자 의학(Experimental & Molecular Medicine)
실험 및 분자 의학(EMM)은 한국 최초의 생화학 학술지(1964년 창간)이며 2013년에 Nature Publishing group을 통한 국제 저널로 재창간되었다. 인간 질병에 대한 중개 의학을 목표로 하며, 분자생물학 기법을 사용한 병리 연구를 주로 다루는 학술지이다. Impact factor는 2021년 기준 11.590이다.
6. 헤마톨로지카(Haematologica)
헤마톨로지카(Haematologica)는 1920년에 창간된 페라타-스톨티 재단 (Ferrata-Storti Foundation)에서 발행하는 학술지로, 혈액학과 관련된 포괄적인 임상 및 중개 연구에 대해 다룬다. Impact factor는 2021년 기준 11.04 이다.